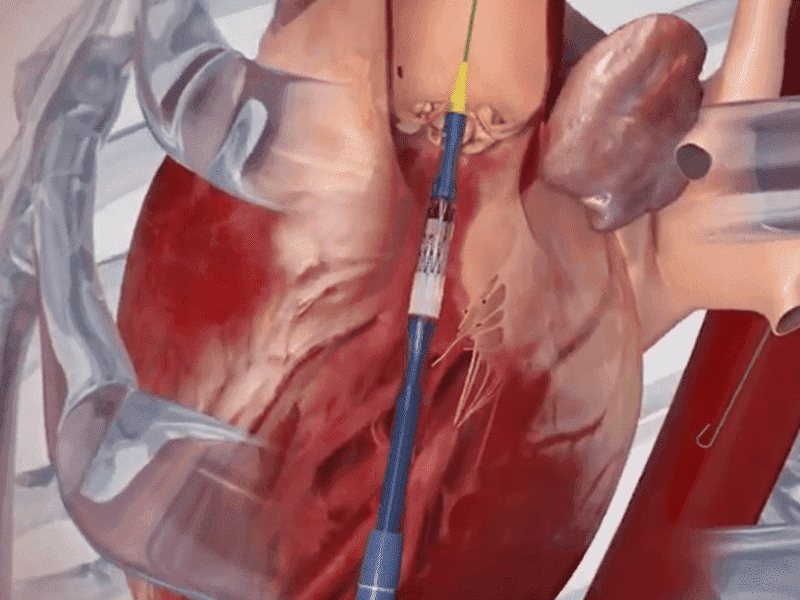
Tanto la válvula auto expandible Evolut R como su competidora directa, la de balón expandible Sapien 3, recibieron la autorización para ser indicadas en pacientes de bajo riesgo el 16 de agosto de 2019 en un anuncio largamente esperado.
La Administración Federal de Drogas y Alimentos (FDA) aprobó y expandido tanto la indicación de la serie Evolut (Medtronic) como la Sapien 3 y la Sapien Ultra (Edwards Lifesciences) para tratar pacientes con estenosis aórtica severa y bajo riesgo quirúrgico.
Le puede interesar:
Sociedad de Cardiología insistirá con ARS en mejorar honorarios
Las válvulas están ahora aprobadas para tratar todo el espectro de riesgo, desde pacientes descartados para cirugía, aquellos de riesgo intermedio y, desde el 16 de agosto, los de bajo riesgo también.
La indicación de expandir el dispositivo producido por Medtronic se basa en los resultados del estudio Evolut Low-Risk publicado a principios de año en NEJM y presentado en las sesiones científicas del ACC.
Según destaca la Sociedad Latonoamericana de Cardiología Intervencionista, en este trabajo se randomizaron mil 468 pacientes a TAVI o cirugía. Más del 96% de los pacientes recibieron los modelos Evolut R o Evolut Pro.
El end point primario de muerte y stroke incapacitante a los 24 meses (end point primario) fue del 5.3% para el brazo que recibió TAVI vs 6.7% para el que recibió cirugía. Estos números alcanzaron el objetivo de no inferioridad.
Le puede interesar:
Sodocardio orienta sobre el síndrome coronario agudo
Core Valve, Evolut R y Evolut Pro fueron aprobadas para pacientes de riesgo intermedio en julio de 2017. Core Valve fue aprobada para pacientes de riesgo extremo y alto en 2014, incorporándose en esta indicación los nuevos modelos en 2015 y 2017, respectivamente.
La indicación de expandir la Sapien 3 y la Sapien Ultra vino de la mano del Partner 3, que también fue presentado en las sesiones científicas de la ACC y publicado simultáneamente en NEJM.
Le puede interesar:
Sodocardio reacciona ante reportajes del periódico Hoy
En el trabajo se incluyeron mil pacientes de bajo riesgo y se observó que el TAVI se asoció significativamente a un menor riesgo de muerte de cualquier causa, stroke o re-hospitalización comparado con la cirugía.
La Sapien XT y la Sapien 3 fueron aprobadas para pacientes de riesgo intermedio en agosto 2016.
El TAVI llegó a oídos de los pacientes, pero también de los financiadores de salud y probablemente ofrecer el TAVI para todo el espectro de pacientes no sea costo efectivo para muchas regiones.






