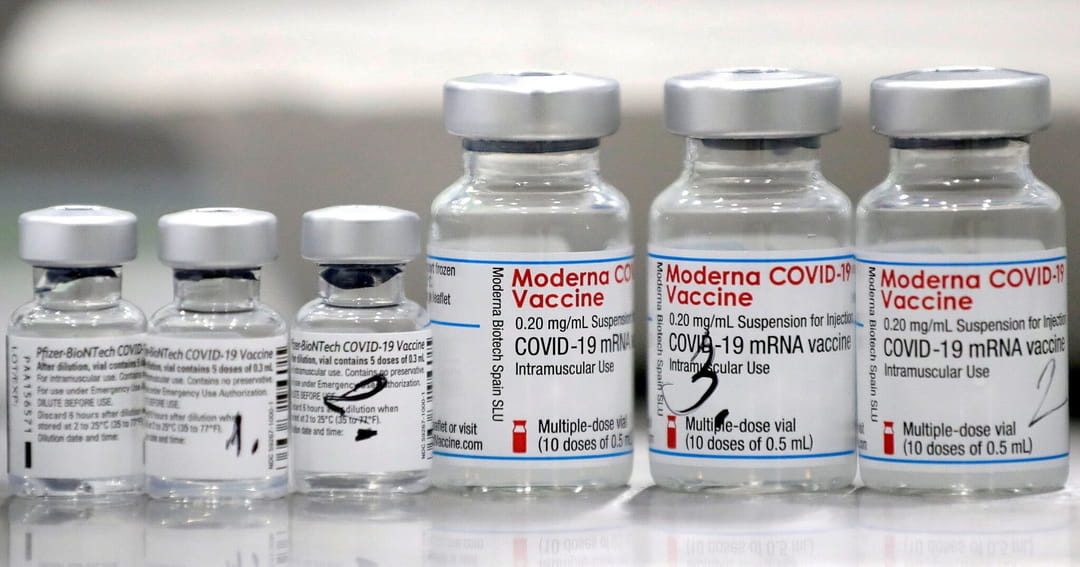
 Europa.- El Comité de Medicamentos Humanos (CHMP) de la Agencia Europea del Medicamento (EMA) ha otorgado la autorización condicional de comercialización a la vacuna de Pfizer y BioNTech contra el COVID-19.
Europa.- El Comité de Medicamentos Humanos (CHMP) de la Agencia Europea del Medicamento (EMA) ha otorgado la autorización condicional de comercialización a la vacuna de Pfizer y BioNTech contra el COVID-19.
La autorización otorgada permite la aplicación del antídoto en personas de más de 16 años.
Le puede interesar:
Estudio revela tiempo de permanencia de anticuerpos en pacientes covid-19
El anuncio fue realizado este lunes por la directora ejecutiva de la EMA, Emer Cooke, tras la reunión del comité para evaluar la vacuna.
“La evaluación científica de la EMA se basa en la fuerza de las pruebas científicas sobre la seguridad, calidad y eficacia de la vacuna, y nada más. Las pruebas demuestran de forma convincente que los beneficios son mayores que los riesgos de esta vacuna”, señaló Cooke.