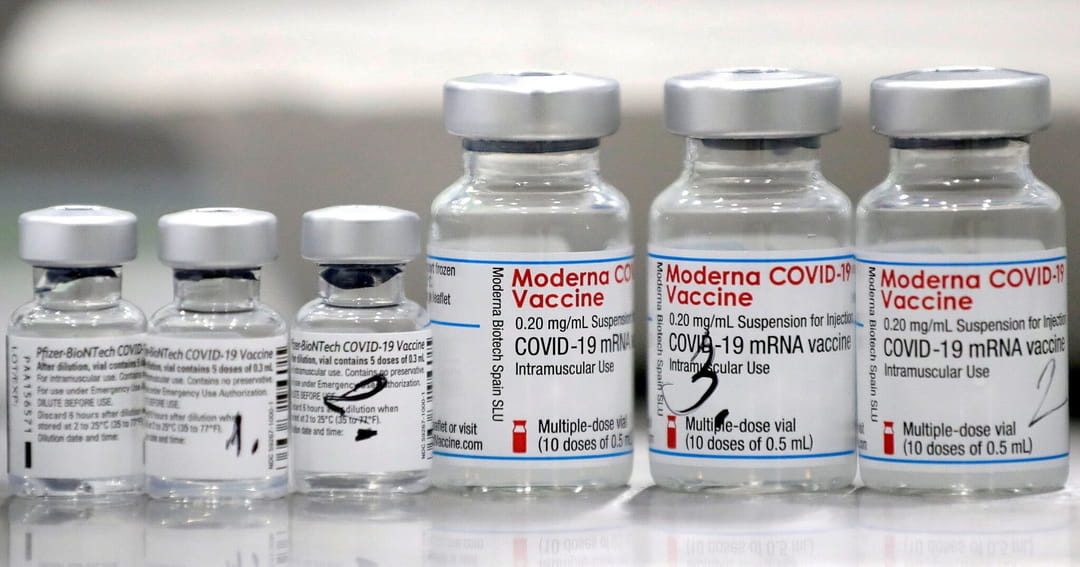
 Río de Janeiro.- La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil autorizó que se realicen en el país ensayos clínicos con voluntarios de una nueva vacuna contra el COVID-19 elaborada por el laboratorio chino Sichuan Clover Biopharmaceuticals.
Río de Janeiro.- La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil autorizó que se realicen en el país ensayos clínicos con voluntarios de una nueva vacuna contra el COVID-19 elaborada por el laboratorio chino Sichuan Clover Biopharmaceuticals.
Según informó el regulador en un comunicado, la vacuna candidata (SCB-2019) se administra con un intervalo de 22 días entre las dos dosis y en Brasil se realizará la fase 2/3 de los test, que planea incluir a 12.100 voluntarios, distribuidos entre Rio Grande do Sul (sur), Rio Grande do Norte (noreste) y Río de Janeiro (sureste).
Le puede interesar:
CR continúa esquema de vacunación contra covid-19
En total, se plantea testar la vacuna en 22 mil voluntarios distribuidos entre países de Latinoamérica, además de Sudáfrica, Bélgica, China, España, Polonia y Reino Unido.
Para esta autorización, la Anvisa analizó los datos de las etapas anteriores de desarrollo de los productos, incluyendo estudios no clínicos in vitro y en animales, así como los datos preliminares de estudios clínicos en marcha.
“Los resultados obtenidos hasta el momento demostraron un perfil de seguridad aceptable de las vacunas candidatas”, destacó la agencia brasileña.
Este es el sexto estudio de la vacuna contra el nuevo coronavirus autorizado en Brasil, después de los de AstraZeneca, Sinovac, Pfizer, Janssen y Medicago R&D, según destaca https://mundo.sputniknews.com.