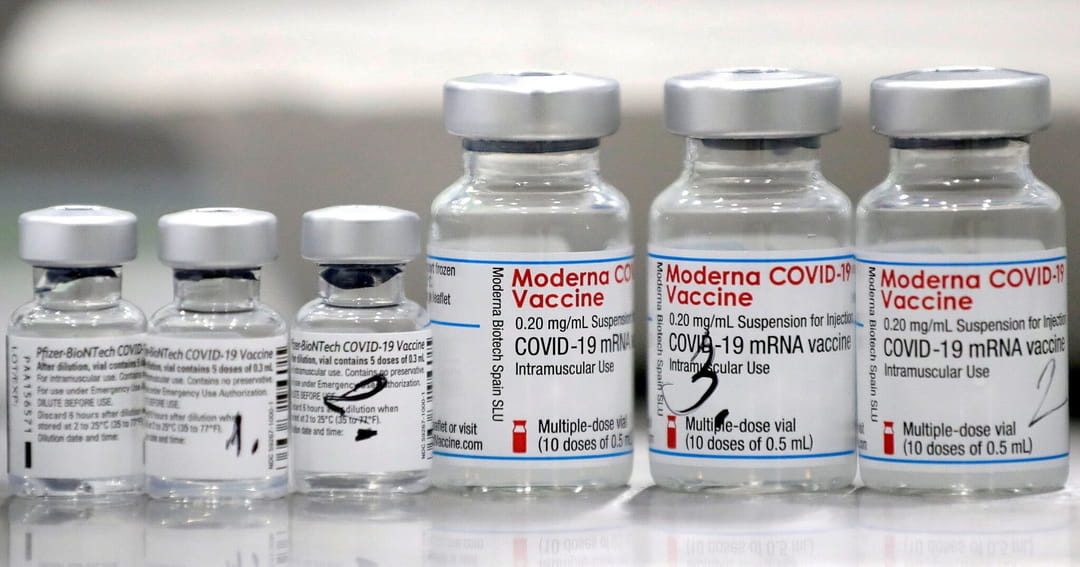
 San José.- Actualmente el gobierno de Costa Rica realizó un acuerdo con Pfizer y BioNTech con la finalidad de garantizar el suministro de la vacuna y de esta manera ayudar a enfrentar la pandemia de COVID-19 que se vive en el país.
San José.- Actualmente el gobierno de Costa Rica realizó un acuerdo con Pfizer y BioNTech con la finalidad de garantizar el suministro de la vacuna y de esta manera ayudar a enfrentar la pandemia de COVID-19 que se vive en el país.
En este sentido es importante señalar que el programa BNT162 se basa en la tecnología de ARNm, patentada por BioNTech y está respaldado por las capacidades globales de desarrollo y fabricación de vacunas de Pfizer.
Le puede interesar
Así comienza la semana en covid-19 en Costa Rica
En julio, dos de las cuatro candidatas a vacunas que investigaban las compañías, BNT162b1 y BNT162b2, recibieron la designación de Vía Rápida por parte de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). Esta designación se concedió sobre la base de datos preliminares de los estudios en fase 1/2 que se están llevando a cabo actualmente en Estados Unidos y Alemania, así como de estudios de inmunogenicidad animal.
El 27 de julio, Pfizer y BioNTech anunciaron que luego de un análisis exhaustivo de los datos preclínicos y clínicos de los ensayos clínicos de fase 1/2, y en consulta con el Centro de Evaluación e Investigación Biológica de la FDA (CBER) y otros organismos reguladores mundiales, las empresas seleccionaron la vacuna candidata BNT162b2 para pasar a un estudio de fase 2/3.
La BNT162b2 codifica una glicoproteína pico de tamaño completo (S) del SARS-CoV-2 optimizada, que es el objetivo de los anticuerpos neutralizadores del virus.
Le puede interesar
Laboratorio Molecular asume 45% de las pruebas de covid-19 en CR
Sobre el estudio fase 2/3
En la última etapa del ensayo, las compañías estudiarán una dosis de 30 µg en un régimen de dos dosis entre 44.000 participantes de 16 a 85 años. Se espera incluir aproximadamente 120 sitios en 3 países, incluyendo regiones donde se prevé una importante transmisión del SARS-CoV-2.
Asumiendo el éxito clínico, Pfizer y BioNTech están en camino de conseguir la revisión regulatoria de BNT162b2 antes de fin de año y, si se obtiene la autorización o aprobación regulatoria, planean suministrar hasta 100 millones de dosis en todo el mundo para fines de 2020 y aproximadamente 1.3 billones de dosis para fines de 2021.
La vacuna candidata BNT162 no está actualmente aprobada para su distribución en ningún lugar del mundo. Ambos colaboradores están comprometidos con el desarrollo de estas nuevas vacunas con datos preclínicos y clínicos al frente de toda su toma de decisiones.