 La vacuna contra el nuevo coronavirus de Johnson & Johnson empezó la etapa final de pruebas clínicas el lunes 22 de septiembre. Este medicamento experimental tiene importantes ventajas sobre otras en desarrollo debido a que podría requerir solo una dosis, en lugar de dos y a que no debe guardarse en temperaturas bajo cero centígrados.
La vacuna contra el nuevo coronavirus de Johnson & Johnson empezó la etapa final de pruebas clínicas el lunes 22 de septiembre. Este medicamento experimental tiene importantes ventajas sobre otras en desarrollo debido a que podría requerir solo una dosis, en lugar de dos y a que no debe guardarse en temperaturas bajo cero centígrados.
De acuerdo con el director científico de la farmacéutica, Dr. Paul Stoffels, la compañía podrá determinar para finales de este año si la vacuna es efectiva y segura. En los próximos días, dijo, la empresa publicará documentos con datos de las primeras fases de las pruebas clínicas.
Es en la llamada fase 3 que se comparan los efectos del medicamento experimental con los de la sustancia placebo, lo que mide la eficacia del producto a gran escala en miles de voluntarios. Eso permitirá, entre otras cosas, confirmar la hipótesis de que no requerirá más de una dosis. De tener resultados positivos en esta etapa, la propagación del virus SARS-CoV2 podría frenarse de manera considerable.
Le puede interesar
Simposio latinoamericano online COVID-19
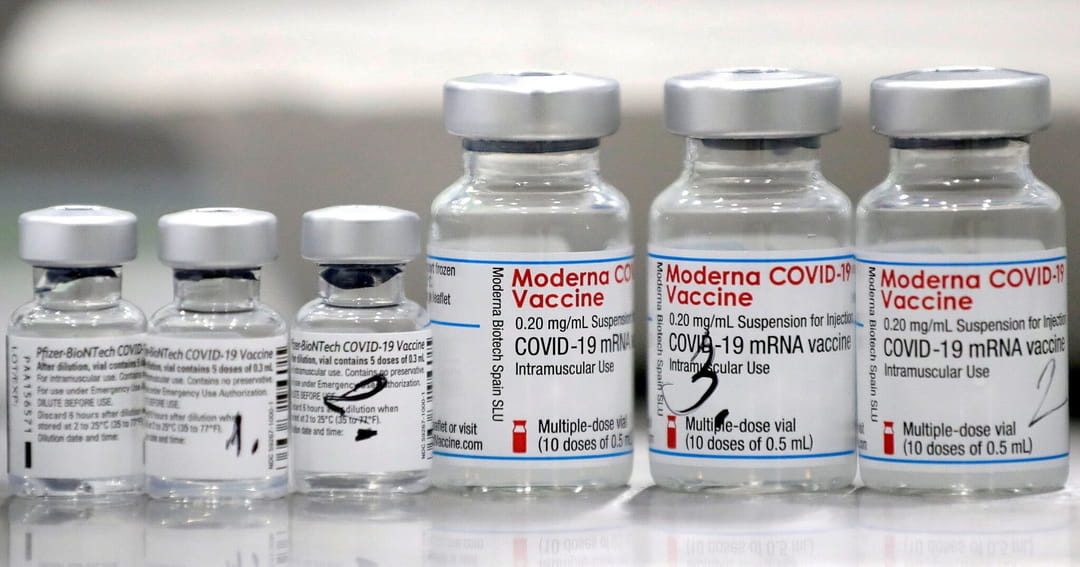
Johnson & Johnson es el cuarto grupo farmacéutico en comenzar la fase 3 de ensayos clínicos de su vacuna experimental en Estados Unidos. La empresa de biotecnología Moderna fue la primera en Estados Unidos, en julio, en comenzar la fase 3. Le siguieron Pfizer y su socio BioNTech, luego llegó AstraZeneca.
La etapa de pruebas que realizará Johnson & Johnson será la más grande porque participarán 60.000 voluntarios de tres continentes a los que se les suministrará una sola dosis.
Johnson & Johnson usa adenovirus para “transportar” un gen del coronavirus hasta las células humanas que, a vez producen proteínas del coronavirus. Esas proteínas, que no son el virus en sí mismo, pueden preparar potencialmente al sistema inmunológico para combatir una posterior infección causada por el letal virus.
Los adenovirus son una familia de virus que infecta tanto a humanos como a otros animales, que pueden provocar infecciones en las vías respiratorias, conjuntivitis, cistitis hemorrágica y gastroenteritis.
Las vacunas a partir de adenovirus debe mantenerse refrigeradas pero no congeladas, a diferencia de las otras dos medicinas experimentales que ya están en etapas avanzadas (realizadas por Moderna y Pfizer), las cuales dependen de un material genético conocido como mRNa. El requisito de congelar la vacuna puede complicar su distribución, especialmente a lugares sin condiciones.
Le puede interesar
PAHO-WHO desarrolla webinar en pro de sistemas de protección social universal
Johnson & Johnson, que anunció su compromiso de distribuir la vacuna sin obtener beneficios, enfatizó que “continuará aumentando su capacidad de producción” para poder entregar 1.000 millones de dosis de vacuna al año.
Anthony Fauci, director del Instituto Americano de Enfermedades Infecciosas, aseguró en un comunicado que es un hecho “sin precedentes” que cuatro vacunas experimentales estén en una fase tan avanzada solo ocho meses después de haberse identificado el nuevo coronavirus.
“Es probable que se necesiten varias formas de vacunación para satisfacer las necesidades globales”, advirtió Fauci.